
この製品のお知らせ
製品基本情報
-
ハイゼントラ20% 皮下注1g/5mL
-
ハイゼントラ20% 皮下注2g/10mL
-
ハイゼントラ20%皮下注4g/20mL
-
ハイゼントラ20%皮下注1g/5mLシリンジ
-
ハイゼントラ20%皮下注2g/10mLシリンジ
-
ハイゼントラ20%皮下注4g/20mLシリンジ
製品の供給状況
| 製品名 | 出荷対応の状況 | 出荷量の状況 | 解除見込み時期 | |
|---|---|---|---|---|
| ハイゼントラ20% 皮下注1g/5mL | ①通常出荷 | Aプラス.出荷量増加 | ||
| ハイゼントラ20% 皮下注2g/10mL | ②限定出荷(自社の事情) | A.出荷量通常 | 詳細 | |
| ハイゼントラ20%皮下注4g/20mL | ②限定出荷(自社の事情) | A.出荷量通常 | 詳細 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | ①通常出荷 | A.出荷量通常 | ||
| ハイゼントラ20%皮下注2g/10mLシリンジ | ①通常出荷 | A.出荷量通常 | ||
| ハイゼントラ20%皮下注4g/20mLシリンジ | ①通常出荷 | A.出荷量通常 | ||
【出荷対応の状況】
①通常出荷 :全ての受注に対応できている、かつ十分な在庫量が確保できている状況
【出荷量の状況】
Aプラス. 出荷量増加 : 比較対象期間の出荷量又は市場予測による予定出荷量の概ね110%以上の出荷状況
A. 出荷量通常 : 比較対象期間の出荷量又は市場予測による予定出荷量の概ね90%以上110%未満の出荷状況
詳細情報
| 剤形 | 注射剤(液剤) | |
|---|---|---|
| 製剤の規制区分 | 特定生物由来製品、処方箋医薬品注) 注)注意−医師等の処方箋により使用すること | |
| 規格・含量 | ハイゼントラ20%皮下注 1g/5mL:1バイアル中 人免疫グロブリンG 1,000mg | |
| ハイゼントラ20%皮下注 2g/10mL:1バイアル中 人免疫グロブリンG 2,000mg | ||
| ハイゼントラ20%皮下注 4g/20mL:1バイアル中 人免疫グロブリンG 4,000mg | ||
| ハイゼントラ20%皮下注 1g/5mL シリンジ:1シリンジ中 人免疫グロブリンG 1,000mg | ||
| ハイゼントラ20%皮下注 2g/10mL シリンジ:1シリンジ中 人免疫グロブリンG 2,000mg | ||
| ハイゼントラ20%皮下注 4g/20mL シリンジ:1シリンジ中 人免疫グロブリンG 4,000mg | ||
| 一般名 | 和名:pH4 処理酸性人免疫グロブリン(皮下注射) 洋名:pH4-Treated Normal Human Immunoglobulin(Subcutaneous injection) | |
| 製造販売承認年月日 薬価基準収載・ 販売開始年月日 (ハイゼントラ20%皮下注) | 製造販売承認年月日:2013年9月27日 薬価基準収載年月日:2013年11月19日 販売開始年月日:2014年1月30日 | |
| 製造販売承認年月日 薬価基準収載・ 販売開始年月日 (ハイゼントラ20%皮下注シリンジ) | 製造販売承認年月日:2024年1月17日 薬価基準収載年月日:2024年6月14日 販売開始年月日:2024年8月8日(4g/20mL)、2024年 8月28日(1g/5mL, 2g/10mL) | |
| 貯法 | 凍結を避けて2~25℃で保存 | |
| 有効期間 | 製造日から30箇月 | |
| 承認番号 | 1g/5mL | 22500AMX01830 |
| 2g/10mL | 22500AMX01831 | |
| 4g/20mL | 22500AMX01832 | |
| 1g/5mLシリンジ | 30600AMX00023 | |
| 2g/10mLシリンジ | 30600AMX00024 | |
| 4g/20mLシリンジ | 30600AMX00025 | |
| 組成 | 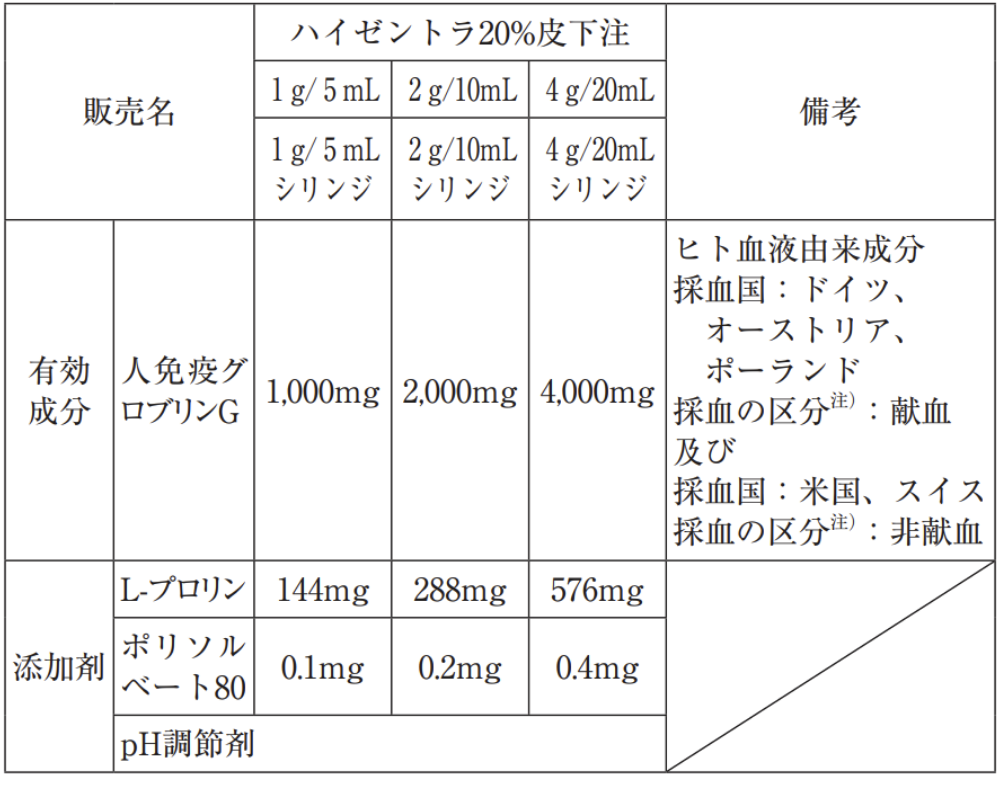 注)電子添文内「献血又は非献血の区別の考え方」参照 | |
| 効能又は効果 | ○無又は低ガンマグロブリン血症 ○慢性炎症性脱髄性多発根神経炎の運動機能低下の進行抑制(筋力低下の改善が認められた場合) | |
| 用法及び用量 | 〈無又は低ガンマグロブリン血症〉 通常、人免疫グロブリンGとして50~200mg(0.25~1mL)/kg体重を週1回皮下投与する。2週間に1回投与する場合には、1週あたりの用量の2倍量(100~400mg(0.5~2mL)/kg体重)を皮下投与する。 なお、患者の状態に応じて、1週もしくは2週あたりの投与量及び投与回数は適宜増減する。 〈慢性炎症性脱髄性多発根神経炎の運動機能低下の進行抑制(筋力低下の改善が認められた場合)〉 通常、成人には人免疫グロブリンGとして 1 週あたり200mg(1mL)/kg体重を1日又は連続する2 日で分割して皮下投与するが、患者の状態に応じて、最大400mg(2mL)/kg体重から投与を開始することもできる。なお、維持用量は200~400mg/kg体重で適宜増減する。 | |
各種コード
| 統一商品コード | ハイゼントラ20%皮下注1g/5mL | 731142284 |
|---|---|---|
| ハイゼントラ20%皮下注2g/10mL | 731142291 | |
| ハイゼントラ20%皮下注4g/20mL | 731142307 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 731142406 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 731142413 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 731142420 | |
| JANコード | ハイゼントラ20%皮下注1g/5mL | 4987731142284 |
| ハイゼントラ20%皮下注2g/10mL | 4987731142291 | |
| ハイゼントラ20%皮下注4g/20mL | 4987731142307 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 4987731142406 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 4987731142413 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 4987731142420 | |
| 日本標準商品分類番号 | 876343 | |
| 薬効分類コード | 6343 | |
| 薬価基準収載医薬品コード (YJコード) | ハイゼントラ20%皮下注1g/5mL | 6343439A1024 |
| ハイゼントラ20%皮下注2g/10mL | 6343439A2020 | |
| ハイゼントラ20%皮下注4g/20mL | 6343439A3027 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 6343439G1027 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 6343439G2023 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 6343439G3020 | |
| GS1コード 調剤包装単位 | ハイゼントラ20%皮下注1g/5mL | 04987731900280 |
| ハイゼントラ20%皮下注2g/10mL | 04987731900297 | |
| ハイゼントラ20%皮下注4g/20mL | 04987731900303 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 04987731900808 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 04987731900815 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 04987731900822 | |
| GS1コード 販売包装単位 | ハイゼントラ20%皮下注1g/5mL | 14987731142281 |
| ハイゼントラ20%皮下注2g/10mL | 14987731142298 | |
| ハイゼントラ20%皮下注4g/20mL | 14987731142304 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 14987731142403 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 14987731142410 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 14987731142427 | |
| GS1コード 元梱包装単位 | ハイゼントラ20%皮下注1g/5mL | 24987731142288 |
| ハイゼントラ20%皮下注2g/10mL | 24987731142295 | |
| ハイゼントラ20%皮下注4g/20mL | 24987731142301 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 24987731142400 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 24987731142417 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 24987731142424 | |
| 基準コード(HOT13) | ハイゼントラ20%皮下注1g/5mL | 1228809010101 |
| ハイゼントラ20%皮下注2g/10mL | 1228816010101 | |
| ハイゼントラ20%皮下注4g/20mL | 1228823010101 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 1295542010101 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 1295559010101 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 1295566010101 | |
| レセプト電算コード | ハイゼントラ20%皮下注1g/5mL | 622288001 |
| ハイゼントラ20%皮下注2g/10mL | 622288101 | |
| ハイゼントラ20%皮下注4g/20mL | 622288201 | |
| ハイゼントラ20%皮下注1g/5mLシリンジ | 622955401 | |
| ハイゼントラ20%皮下注2g/10mLシリンジ | 622955501 | |
| ハイゼントラ20%皮下注4g/20mLシリンジ | 622955601 | |
バーコードシンボル
| GS1コード 調剤包装単位 | ハイゼントラ®20%皮下注 1g/5mL | ハイゼントラ®20%皮下注 2g/10mL | ハイゼントラ20%皮下注 4g/20mL |
|---|---|---|---|
 |  |  | |
| ハイゼントラ20%皮下注 1g/5mLシリンジ | ハイゼントラ20%皮下注 2g/10mLシリンジ | ハイゼントラ20% 皮下注4g/20mLシリンジ | |
 |  |  |
| GS1コード 販売包装単位 | ハイゼントラ®20%皮下注 1g/5mL | ハイゼントラ®20%皮下注 2g/10mL | ハイゼントラ20%皮下注 4g/20mL |
|---|---|---|---|
 |  |  | |
| ハイゼントラ20%皮下注 1g/5mLシリンジ | ハイゼントラ20%皮下注 2g/10mLシリンジ | ハイゼントラ20%皮下注 4g/20mLシリンジ | |
 |  |  |
薬価
| 薬価(円) | ハイゼントラ20% 皮下注1g/5mL 13,742 ハイゼントラ20% 皮下注2g/10mL 26,449 ハイゼントラ20%皮下注4g/20mL 52,216 ハイゼントラ20%皮下注1g/5mLシリンジ 13,485 ハイゼントラ20%皮下注2g/10mLシリンジ 26,566 ハイゼントラ20%皮下注4g/20mLシリンジ 52,410 ※すべて2026年4月時点 |
|---|---|
| 薬価基準収載医薬品コード | ハイゼントラ20% 皮下注1g/5mL 6343439A1024 ハイゼントラ20% 皮下注2g/10mL 6343439A2020 ハイゼントラ20%皮下注4g/20mL 6343439A3027 ハイゼントラ20%皮下注1g/5mLシリンジ 6343439G1027 ハイゼントラ20%皮下注2g/10mLシリンジ 6343439G2023 ハイゼントラ20%皮下注4g/20mLシリンジ 6343439G3020 |
包装
| 包装 | ハイゼントラ20%皮下注1g/5mL 1バイアル |
|---|---|
| ハイゼントラ20%皮下注2g/10mL 1バイアル | |
| ハイゼントラ20%皮下注4g/20mL 1バイアル | |
| ハイゼントラ20%皮下注 1g/5mLシリンジ 1シリンジ[脱酸素剤入り] | |
| ハイゼントラ20%皮下注2g/10mLシリンジ 1シリンジ[脱酸素剤入り] | |
| ハイゼントラ20%皮下注4g/20mLシリンジ 1シリンジ[脱酸素剤入り] |