
この製品のお知らせ
製品基本情報
-
アナエブリ皮下注200mgペン
製品の供給状況
| 製品名 | 出荷対応の状況 | 出荷量の状況 | 解除見込み時期 | |
|---|---|---|---|---|
| アナエブリ皮下注200mgペン | ①通常出荷 | A.出荷量通常 | ||
【出荷対応の状況】
①通常出荷 :全ての受注に対応できている、かつ十分な在庫量が確保できている状況
【出荷量の状況】
A. 出荷量通常 : 比較対象期間の出荷量又は市場予測による予定出荷量の概ね90%以上110%未満の出荷状況
詳細情報
| 剤形 | 注射剤(液剤) | |
|---|---|---|
| 製剤の規制区分 | 生物由来製品、処方箋医薬品注) 注)注意−医師等の処方箋により使用すること | |
| 規格・含量 | アナエブリ皮下注200mg ペン:1シリンジ中 ガラダシマブ(遺伝子組換え)200mg | |
| 一般名 | 和名:ガラダシマブ(遺伝子組換え)(JAN) 洋名:Garadacimab(Genetical Recombination)(JAN) | |
| 製造販売承認年月日 薬価基準収載 ・販売開始年月日 | 製造販売承認年月日:2025年2月20日 薬価基準収載年月日:2025年4月16日 販売開始年月日:2025年4月18日 | |
| 貯法 | 2~8℃で保存 | |
| 有効期間 | 36箇月 | |
| 承認番号 | 30700AMX00056000 | |
| 組成 | 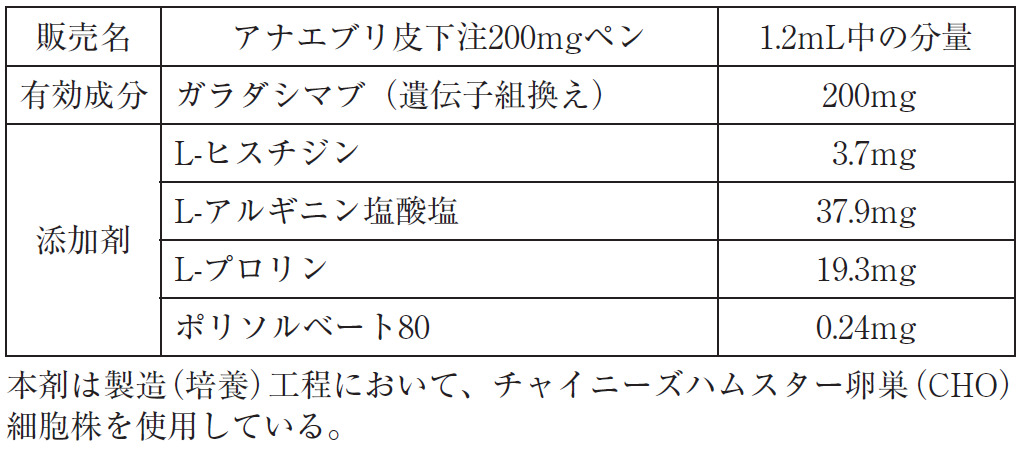 | |
| 効能又は効果 | 遺伝性血管性浮腫の急性発作の発症抑制 | |
| 用法及び用量 | 通常、成人及び12歳以上の小児には、ガラダシマブ(遺伝子組換え)として初回に400mgを皮下投与し、以降は200mgを月1回皮下投与する。 | |
各種コード
| 統一商品コード | 731000263 |
|---|---|
| JANコード | 4987731000263 |
| 日本標準商品分類番号 | 87449 |
| 薬効分類コード | 449 |
| 薬価基準収載医薬品コード (YJコード) | 4490411G1020 |
| GS1コード 調剤包装単位 | 04987731900266 |
| GS1コード 販売包装単位 | 14987731000260 |
| GS1コード 元梱包装単位 | 24987731000267 |
| 基準コード(HOT13) | 1993370010101 |
| レセプト電算コード | 629933701 |
バーコードシンボル
| GS1コード 調剤包装単位 | アナエブリ皮下注200mgペン |
|---|---|
 |
| GS1コード 販売包装単位 | アナエブリ皮下注200mgペン |
|---|---|
 |
薬価
| 薬価(円) | 3,037,716 ※2025年4月時点 |
|---|
包装
| 包装 | 1ペン |
|---|