謹啓
平素より格別のご愛顧を賜りまして、厚く御礼申し上げます。
さて、2019 年 12 月の「医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(昭和 35 年法律第 145 号)」の改正により、2021 年 8 月 1 日から添付文書の電子化の運用が施行されております。これに伴い、弊社製品に同梱していました紙の添付文書は、経過措置期間である 2023 年 7 月 31 日までに順次廃止致します。
最新の電子化された添付文書(電子添文)や関連情報は専用のアプリケーション(「添文ナビ」)で個装箱及びバイアルラベルの GS1 バーコードを読み取ることで、スマートフォンやタブレット端末等からいつでも閲覧できます。
このたび、当該製品につきまして紙の添付文書の同梱廃止とともに下記の通り包装を変更致しますのでご案内申し上げます。
何卒ご理解賜りますよう、宜しくお願い申し上げます。
謹白
記
➢ 4規格共通の変更
- 紙の添付文書同梱廃止に伴い、個装箱及びバイアルラベルの添付文書の表記を添付文書から電子添文へ変更致します。

- 個装箱及びバイアルラベルの表記を一部記載整備致します。
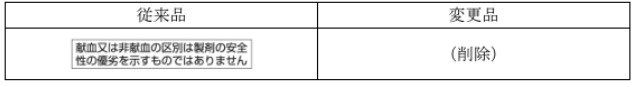
- 個装箱及びバイアルラベルの薬効分類名を電子添文の記載へ統一致します。また、個装箱の貯法の記載を集中表示面のみの記載に致します。

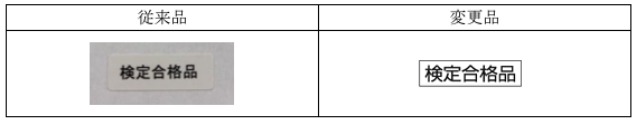
- これまで個装箱に貼付していた検定合格品ラベルを個装箱への印字へ変更致します。
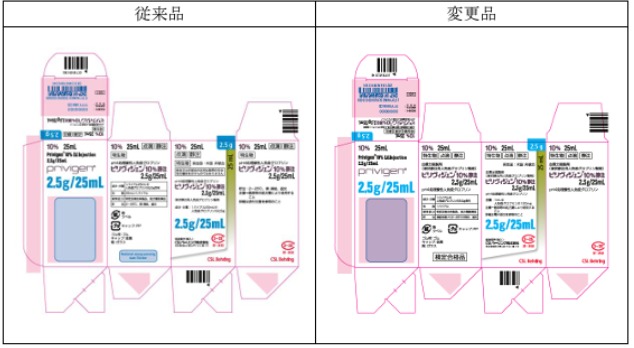
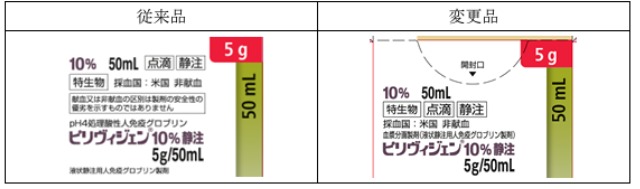
参照画像:ピリヴィジェン10%静注2.5g/25mL
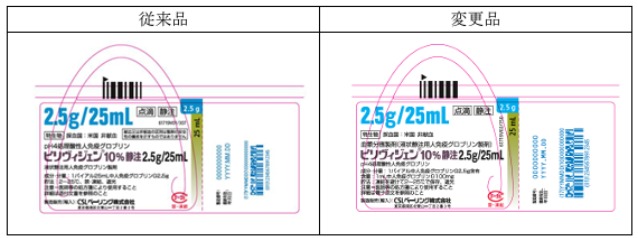
➢ ピリヴィジェン10%静注5g/50mL及びピリヴィジェン10%静注10g/100mLの2規格に関する追加の変更
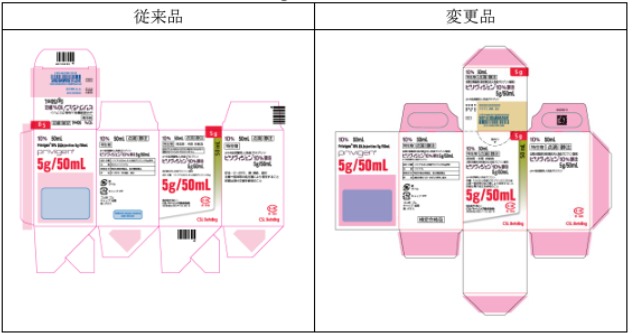
- 個装箱にミシン目を追加し、「開封口」の表示を致します。
- 個装箱のフラップ及び底面の形状を変更致します。
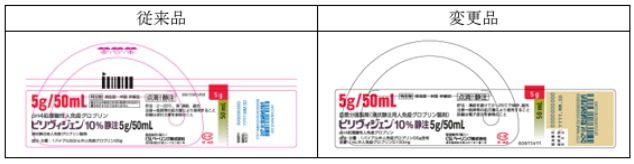
参照画像:ピリヴィジェン10%静注5g/50mL
➢ 変更品の製造番号及び出荷予定時期
| 製品名 | 包装 | 統一商品コード | 製造番号 | 出荷予定時期 |
| ピリヴィジェン10%静注2.5g/25mL | 1 バイアル | 731142345 | 未定 | 2023年9月初旬より順次出荷 |
| ピリヴィジェン10%静注5g/50mL | 1 バイアル | 731142352 | P100544331 | 2023年6月下旬より順次出荷 |
| ピリヴィジェン10%静注10g/100mL | 1 バイアル | 731142369 | P100566482 | 2023年8月上旬より順次出荷 |
| ピリヴィジェン10%静注20g/200mL | 1 バイアル | 731142376 | P100544330 | 2023年6月下旬より順次出荷 |
※個装箱のサイズ変更はありません。
※ピリヴィジェン10%静注5g/50mL及びピリヴィジェン10%静注10g/100mLに関しては段ボールの入り数が10本から20本へ変更になります。
※出荷予定時期は当該案内作成時点の予定であるため、実際の出荷時期との相違が生じる場合がございますが、ご了承の程お願い申し上げます。
※変更品の製造番号は、紙の添付文書の同梱を廃止する製造番号と同一です。弊社ホームページに順次更新情報を掲載しておりますので、ご参照くださいますようお願い申し上げます。
以上